Регистрационное удостоверение на медицинские изделия — это официальный документ, подтверждающий соответствие закупаемой продукции медицинского назначения критериям, установленным законодательством РФ. В статье мы поговорим о роли этого документа в государственных закупках по 44-ФЗ, узнаем особенности его получения и необходимость предоставления в составе заявки на участие в закупочной процедуре.

- Что такое регистрационное удостоверение на медицинские изделия?
- Как получить регистрационное удостоверение?
- Что указывать в заявлении?
- Необходимые документы для госрегистрации медизделия
- Когда нужно предоставлять регистрационное удостоверение?
- Можно ли не предоставлять копию регистрационного удостоверения заказчику?
- Как проверить регистрационное удостоверение?
- Форма регистрационных удостоверений в 2020 году
Что такое регистрационное удостоверение на медицинские изделия?
В настоящее время всю продукцию медицинского назначения необходимо регистрировать в порядке, предусмотренном законодательством, и по установленным в нем правилам. Без такой регистрации продавать медицинские изделия на территории Российской Федерации категорически запрещено (ст.38 323-ФЗ от 21.11.2011 г.).
Наличие специализированного регистрационного удостоверения (РУ) дает возможность заказчику проверить, прошел ли товар процедуру фиксации. Порядок действий утвержден в Правилах госрегистрации медицинских изделий (Постановление Правительства РФ № 1416 от 27.12.2012 г.).
Регистрационное удостоверение на медизделие выдается на официальном бланке и подтверждает, что данное медицинское изделие зарегистрировано надлежащим образом согласно действующему законодательству.
Только после получения разрешительного документа, исполнитель получает легальное право на реализацию той или иной медпродукции внутри нашей страны.
Как получить регистрационное удостоверение?
Функции регистрирующего органа выполняет Федеральная служба по надзору в сфере здравоохранения.
Основанием для госрегистрации медпродукции являются результаты различных исследований и испытаний: технических, токсикологических, клинических. После чего выдается РУ, которое действует бессрочно.
Соискатель обязан оплатить госпошлину, информация о ней запрашивается регистрирующим органом согласно законодательству.
Претендовать на получение документа может разработчик медтовара, его производитель (либо уполномоченный производитель). Для этого в Федеральную службу по надзору необходимо направить заявление и пакет документов в соответствии с порядком, утвержденным в п.8 и 9 Постановления Правительства РФ № 1416 от 27.12.2012 г.
Что указывать в заявлении?
- название медицинской единицы (также указываются принадлежности, с которыми изделие применяется по назначению); товарный знак и другие параметры изделия, если они нанесены на упаковку;
- сведения о разработчике: наименование, организационно-правовая форма, адрес местонахождения, телефон, электронная почта (для юрлица); или ФИО, паспорт, адрес проживания, телефон, электронная почта (для ИП);
- сведения о производителе: наименование, организационно-правовая форма, адрес местонахождения, телефон, электронная почта (для юрлица); или ФИО, паспорт, адрес проживания, телефон, электронная почта (для ИП);
- сведения об уполномоченном лице производителя: наименование, организационно-правовая форма, адрес местонахождения, телефон, электронная почта (для юрлица); или ФИО, паспорт, адрес проживания, телефон, электронная почта (для ИП);
- сведения о лице, которому может быть выдано РУ: наименование, организационно-правовая форма, адрес местонахождения, телефон, электронная почта (для юрлица); или ФИО, паспорт, адрес проживания, телефон, электронная почта (для ИП);
- место производства продукции;
- назначение медтовара (как указал производитель);
- вид медтовара по классификатору медизделий;
- класс потенциального риска по классификатору медизделий;
- код продукции по Общероссийскому классификатору видов экономической деятельности;
- информация о способе получения РУ и сведений по процедуре регистрации.
Требовать иных сведений в заявлении регистрирующий орган не имеет права.
Необходимые документы для госрегистрации медизделия
- подтверждение полномочий представителя изготовителя товара (копия документа);
- нормативные документы на продукцию;
- технические документы изготовителя на продукцию;
- документы об эксплуатации изделия от производителя, в том числе, инструкция по применению;
- фотографии общего вида изделия с принадлежностями для его использования по назначению (фото не менее 18 x 24 см.);
- документы о результатах технических испытаний, токсикологических исследований (в случае контакта продукции с организмом человека);
- документы о результатах испытаний, устанавливающих тип средств измерений (для средств измерений));
- опись документов;
- информация о клинической эффективности и безопасности (для изделий 1 класса);
- проект плана клинических испытаний с обоснованиями (при наличии);
- информация о наличии разрешений на ввоз продукции для последующей госрегистрации (для иностранной продукции);
- подтверждения качества медтовара (копии документов);
Требовать иных документов регистрирующий орган не имеет права.
Заявление и весь пакет документов предоставляются соискателем в регистрирующий орган на бумажном носителе непосредственно или по почте, либо в электронной форме и подписанные электронной подписью.
Когда нужно предоставлять регистрационное удостоверение?
Ст. 31 44-ФЗ дает право заказчикам устанавливать требования к предоставляемой участниками документации. При закупке медицинских изделий организаторы торгов прописывают требование о предоставлении соответствующего свидетельства, чтобы самим подстраховаться от закупки ненадлежащей продукции.
Следует отметить, что при проведении запроса котировок требовать РУ в составе заявки запрещено (ст.73 44-ФЗ). В Распоряжении Правительства РФ № 471-р от 21.03.2016 г. утвержден аукционный перечень медизделий, которые надлежит закупать только путем проведения электронного аукциона.
Согласно п.3 ч.5 ст.66 44-ФЗ, если к закупаемой продукции законодательством установлены какие-либо требования, то они должны быть указаны в закупочной документации стороной заказчика. Если при проведении электронного аукциона необходимо представлять документы, подтверждающие качество товара (лицензии, свидетельства, сертификаты), то их копии предоставляются в составе второй части заявки.
Требовать предоставление соответствующего свидетельства на товар в составе 2-й части заявки это не просто право заказчика – это его обязанность, неисполнение которого считается нарушением ст.66 44-ФЗ и ст.38 323-ФЗ (Письмо № АД/43043/14 от 23.10.2014 г.).
Закупочная комиссия проверяет документацию, представленную участником. В ходе проверки сверяется продукция, указанная в первой части заявки, с копиями регистрационных удостоверений из второй части заявки. Если данные сходятся, то заявка признается соответствующей требованиям, если нет – отклоняется.
Специалисты закупочной комиссии также должны проверять каждое наименование медицинского товара, указанного в РУ, чтобы не допустить попадания в него какого-то конкретного незарегистрированного изделия. Каждый товар в перечне в составе заявки должен совпадать с каждым товаром в регистрационном свидетельстве. При этом закупаемый товар обязательно должен отдельно указываться в приложении к РУ (Решение Свердловского УФАС по делу № 8444-З от 22.06.2015 г.).
Кроме обязательства требовать копии РУ, заказчик должен их получить на руки в ходе поставки и приемки. Исполнитель обязан вместе с товаром передать заказчику всю документацию (сертификаты, свидетельства, техпаспорт, лицензии), согласно п.2 ст.456 ГК РФ.
Можно ли не предоставлять копию регистрационного удостоверения заказчику?
В Письме ФАС России от 23.10.2014 г. № АД/43043/14 говорится, что заказчик может запросить только информацию о наличии РУ. Сами же сведения о продукции можно найти в соответствующих реестрах:
— в Государственном реестре лекарственных средств (ГРЛС),
— в Государственном реестре медицинских изделий (ГРМИ).
Если участник предоставит только информацию о регистрационном удостоверении (а не его копию), а заказчик на основании этого отклонит заявку, то он нарушит положения 44-ФЗ.
Как проверить регистрационное удостоверение?
На момент проведения закупки регистрационное удостоверение должно быть с актуальным сроком действия. Этот пункт заказчик также прописывает в документации.
Свидетельство, которое участник предоставляет в составе 2-й части заявки, должно быть действительным, даже если ранее в него вносились изменения (п.50 Постановления Правительства РФ № 1416 от 27.12.2012 г.). Заявка участника будет отклонена, если он предоставил свидетельство с истекшим сроком действия (Решение Свердловского УФАС России по жалобе № 145-З от 02.02.2017 г.).
Бывают ситуации, когда необходимо проверить наличие или подлинность удостоверения. Это можно сделать на официальном сайте Росздравнадзора. Это ведомство ведет реестр медицинских изделий (ГРМИ) и компаний-производителей (ч.10 ст.38 323-ФЗ). Реестр подтвердит не только наличие документа, но и предоставит его реквизиты и срок действия.
Необходимо открыть окно с расширенным поиском и ввести все необходимые параметры, а затем нажать «Вывести результаты».
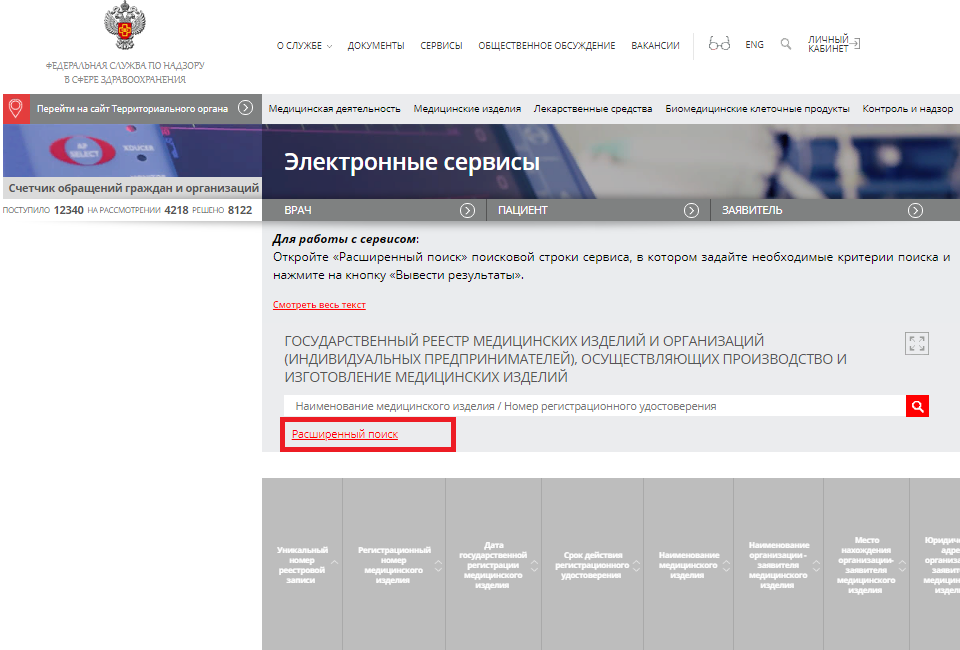
В реестре должна содержаться следующая информация о медицинском изделии:
- название;
- дата регистрации продукции, регистрационный номер и срок действия удостоверения;
- назначение, установленное производителем;
- вид;
- класс потенциального риска применения;
- код Общероссийского классификатора продукции для изделия;
- реквизиты организации – заявителя изделия;
- реквизиты организации — производителя или ФИО индивидуального предпринимателя — производителя;
- адрес производства или изготовления;
- данные о взаимозаменяемости.
Форма регистрационных удостоверений в 2020 году
Законодательство утвердило форму регистрационных удостоверений, действующих в 2020 г. (Приказ Росздравнадзора № 40-Пр/13 от 16.01.2013 г.). Все необходимые приложения являются его неотъемлемой частью.

Все заявки на участие в закупке на приобретение медицинской продукции должны содержать копию как самого регистрационного удостоверения, так и приложения к нему (при наличии). Образец свидетельства выглядит следующим образом:


Приветствую!
Как-то видел в интернете описание комплексной автоматизации бизнес-процессов по обслуживанию домофонов.
Стало надо, но не могу найти.
Там предлагалось перевести базу в 1с-ЖКХ, интегрировать работу по заявкам с картой и что-то процессов общение робота с клиентами с распознаванием голоса ещё какие-то плюшки и всё это что-то в районе 2000 в месяц.
Извиняюсь если пишу не в тему, очень хочу найти эту компанию.